Sistema de pozos de potencial
Actividades
El applet calcula los niveles de energía y representa las funciones de onda de un sistema de pozos de potencial
Se introduce
- el número de pozos, en el control de edición titulado Número de pozos
- la anchura de cada uno de los pozos, en el control de edición titulado Anchura del pozo
- la separación entre los pozos, en el control de edición titulado Separación
- la profundidad de los pozos está fijada en el programa en un valor igual a 5 unidades.
Seleccionando con el puntero del ratón un nivel de energía en el control lista y pulsando en el botón titulado Función de onda, se representa la función de onda correspondiente al nivel seleccionado. El mismo resultado se obtiene haciendo doble-clic sobre el valor del nivel de energía en el control lista situado a la izquierda de la ventana.
Cuando el número de pozos es elevado, el programa tarda cierto tiempo en efectuar el cálculo. Cuando el cursor por defecto cambia a la forma de reloj de arena comienza el proceso de cálculo, y termina cuando aparece de nuevo sobre la ventana del applet el cursor por defecto en forma de puntero.
El átomo.
Introduciendo un uno en el control de edición titulado Número de pozos, se representa un pozo de potencial cuya anchura podemos modificar en el intervalo que va de 0.5 a 3 unidades, introduciendo el valor correspondiente en el control de edición titulado Anchura del pozo.
Vamos a considerar el pozo de potencial como un modelo simplificado de átomo, contaremos el número de niveles de energía, observaremos su distribución y la representación de las funciones de onda correspondientes a cada uno de dichos niveles.
La molécula diatómica
Si el pozo de potencial simple nos da la imagen de un átomo, el pozo de potencial doble es una simplificación de la molécula diatómica.
En el applet, podremos observar que por cada nivel de energía del pozo de potencial simple, se producen dos niveles de energía próximos en el pozo de potencial doble. El nivel más bajo de cada doblete tiene una energía inferior a la correspondiente del pozo de potencial simple y además, es un estado simétrico. Por otra parte, podemos comprobar que el desdoblamiento se incrementa a medida que disminuye la separación entre los pozos.
Los resultados anteriores permiten explicar las facetas esenciales de la unión covalente entre átomos iguales, en el mismo estado, para una distancia de equilibrio entre ambos.
- El estado fundamental tiene una energía inferior a la de los dos átomos aislados, lo que configura una unión estable, la función de onda es simétrica.
- El segundo nivel, tiene una energía superior a la de los átomos aislados, es una unión inestable, la función de onda es antisimétrica.
Comparando la función de onda del átomo en el estado fundamental, y las funciones de onda simétrica y antisimétrica de la molécula diatómica, se pueden establecer las siguientes relaciones aproximadas, base de la teoría conocida por la abreviatura C.L.O.A. (Combinación lineal de orbitales atómicos)
Ψ=Ψ1+Ψ2
para el estado fundamental
Ψ=Ψ1-Ψ2 para el primer nivel
La descripción en términos de probabilidad (cuadrado de la función de onda) nos sugiere que cuando los átomos están alejados, los electrones de cada átomo están ligados a su núcleo respectivo. Cuando la separación es pequeña, en el nivel fundamental, hay una cierta probabilidad, no nula, de encontrar electrones entre ambos átomos, los electrones que participan en la unión no pertenecen ya a un átomo concreto, sino que participan de ambos.
Como actividades de este apartado se proponen:
- Observar los dos primeros niveles de energía de un sistema de dos pozos de potencial y compararlos con el nivel fundamental de un sólo pozo de la misma anchura.
- Comparar la función de onda del estado fundamental de un pozo con las funciones de onda de los dos primeros niveles del sistema de dos pozos de potencial.
Sólido lineal
Un sistema de 3, 4, 5, etc. pozos de potencial representa un modelo simple de los enlaces p de las moléculas conjugadas lineales, tales como los polienos. Los electrones se mueven en una región descrita por un potencial periódico y cada nivel de energía atómico se divide en un número de niveles igual al número de átomos.
En general, en una red de N átomos cada nivel de energía atómico da lugar a N niveles cercanos. Cuando N es grande los niveles de energía están espaciados tan finamente que se puede decir que forman una banda continua de energía.
De acuerdo al Principio de Exclusión de Pauli, cada nivel puede acomodar dos electrones, uno con espín hacia arriba y otro con espín hacia abajo. Una banda de energía correspondiente a un estado atómico dado, puede acomodar un máximo de 2N electrones. Si la banda correspondiente a la capa atómica más externa, la ocupada por los electrones de valencia, no está completamente llena, se denomina banda de conducción, pero si lo está, se denomina banda de valencia, y la banda vacía que queda por encima recibe el nombre de banda de conducción. Dependiendo de la estructura de las bandas, los materiales tienen distintas propiedades eléctricas clasificándose en conductores, aisladores y semiconductores.
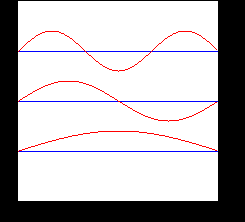 |
La representación gráfica de las funciones de onda de los primeros
niveles de energía de un sistema de muchos pozos de potencial, nos sugiere que se trata
de funciones cuya forma es semejante a los modos
de vibración de una cuerda, pero modulados por la función de onda de un pozo
de potencial. En la figura se esquematiza los tres primeros modos de una cuerda vibrante. |
Como actividades en este apartado se propone observar los niveles de energía y su distribución, para cada sistema de "átomos" que hayamos definido.
- Introducir un número determinado de pozos de potencial y observar el efecto de la modificación de la anchura de los pozos. Observar posteriormente, el efecto de la modificación de la separación entre "átomos" manteniendo fijas sus dimensiones.
- También podrá observar la relación entre la forma de las funciones de onda y de los modos de vibración de una cuerda, el modo fundamental no tiene nodos (no corta al eje horizontal). El segundo armónico, tiene un nodo (corta una vez al eje horizontal), el tercero tiene dos nodos, y así sucesivamente. Lo mismo ocurre con las funciones de onda de un conjunto de pozos de potencial. Podemos saber el orden del nivel de energía contando el número de veces que la función de onda corta al eje horizontal.
- El applet calcula mediante un procedimiento numérico, los niveles de energía. Cuando la diferencia de energía entre dos o más niveles es menor que el paso de exploración que emplea el programa, no se calcula algunos de los niveles. El usuario observará que faltan algunos niveles, es decir, no se suceden de la forma habitual simétrico, antisimétrico, simétrico, etc.